Giải bài tập Hóa học lớp 11 Bài 35: Benzen và đồng đẳng. Một số hiđrocacbon thơm khác
Câu hỏi và bài tập ( trang 160, 161 SGK Hóa học 11)
Bài 1 trang 160 SGK Hóa học 11: Ứng với công thức phân tử C10H8 có bao nhiêu đồng phân hiđrocacbon thơm?
A. 2. B. 3. C. 4. D. 5.
Phương pháp giải :
Bước 1: vẽ vòng thơm => dư bao nhiêu C sẽ để lại làm mạch nhánh
Bước 2: Vẽ nhánh ( chú ý các vị trí o, m, p) để các công thức không bị trùng nhau.
Lời giải chi tiết
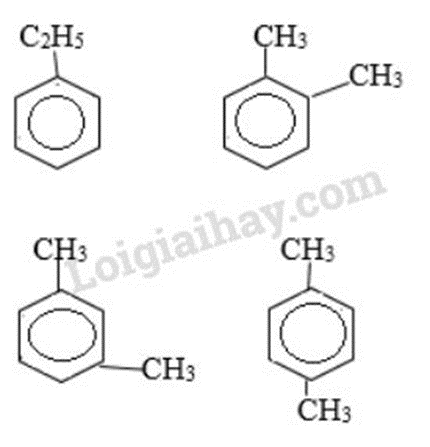
=> có 4 công thức
Đáp án C
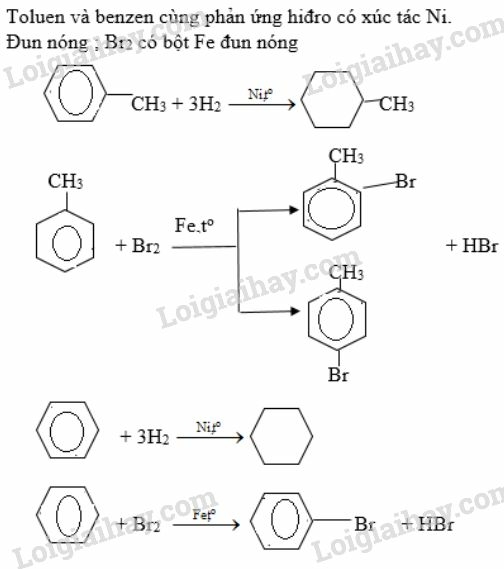
Bài 2 trang 160 SGK Hóa học 11: Toluen và benzen cùng phản ứng được với chất nào sau đây: (1) dung dịch brom trong CCl4; (2) dung dịch kali pemanganat; (3) hiđro có xúc tác Ni, đun nóng; (4) Br2 có bột Fe, đun nóng? Viết phương trình phản ứng hóa học của các phản ứng xảy ra.
Lời giải :
Bài 3 trang 160 SGK Hóa học 11: Viết phương trình hóa học của các phản ứng xảy ra trong mỗi trường hợp sau:
a) Toluen tác dụng với hiđro có xúc tác Ni, áp suất cao, đun nóng.
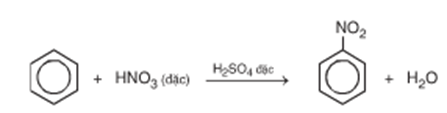
b) Đun nóng benzen với hỗn hợp HNO3 đặc và H2SO4 đặc
Phương pháp giải:
Xem lại lý thuyết về benzen và các ankylbenzen
Lời giải :
a)
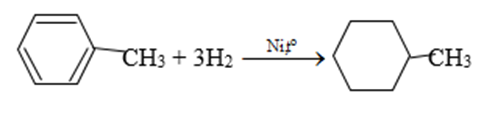
b)
Bài 4 trang 160 SGK Hóa học 11: Trình bày phương pháp hóa học phân biệt các chất: benzen, hex – 1 – en và toluen. Viết phương trình hóa học của các phản ứng đã dùng.
Phương pháp giải :
ta thấy benzen khó tham gia phản ứng cộng, chỉ cộng H2
Hex – 1 -en thuộc dãy anken => dễ tham gia phản ứng cộng Br2, H2, thuốc tím
toluen có tính chất tương tự như benzen nhưng có thêm khả năng làm mất màu dd thuốc tím khi đun nóng
=> chọn ra các tính chất hóa học khác nhau để chọn thuốc thử phân biệt được chúng.
Lời giải :
Trích mỗi chất 1 ít cho ra các ống nghiệm khác nhau và đánh số thứ tự tương ứng
– Nhỏ lần lượt dd brom vào 3 ống nghiệm trên: ống nghiệm nào dd brom nhạt màu là hex – 1 – en. 2 ống còn lại không có hiện tượng là benzen, toluen.
CH2=CH-[CH2]3-CH3 + Br2 (dd màu nâu đỏ) → CH2Br -CHBr -[CH2]3-CH3 ( dd không màu)
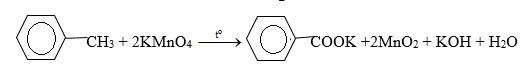
-Nhỏ dung dịch KMnO4 vào hai ống nghiệm còn lại và đun nóng, ống nghiệm nào có hiện tượng mất màu là toluen. Chất còn lại không có hiện tượng gì là benzen
Bài 5 trang 160 SGK Hóa học 11: Hiđrocacbon X là chất lỏng có tỉ khối hơi so với không khí bằng 3,17. Đốt cháy hoàn toàn X thu được CO2 có khối lượng bằng 4,28 lần khối lượng H2O. Ở nhiệt độ thường, X không làm mất màu dung dịch brom. Khi đun nóng, X làm mất màu dung dịch KMnO4.
a) Tìm công thức phân tử và viết công thức cấu tạo của X.
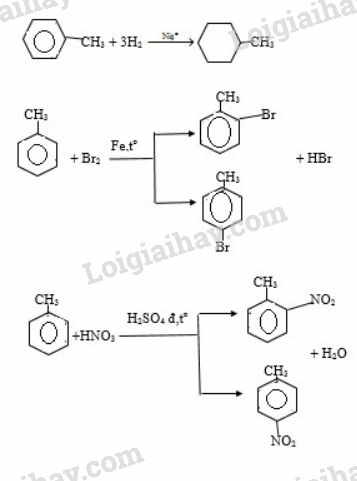
b) Viết phương trình hóa học của phản ứng giữa X và H2 (xúc tác Ni, đun nóng), với brom (có mặt Fe), với hỗn hợp dư của axit HNO3 và axit H2SO4 đậm đặc.
Phương pháp giải:
a)
Gọi CTPT của X là CxHy
MX = 3,17.29 = 92
=> 12x + y = 92 (1)
Từ (1) và (2) => x = ? và y = ?
=> CTPT của X là ? => CTCT X =?
b)
X + H2 (Ni, t0) → phản ứng cộng phá vỡ liên kết I trong vòng benzen
X + Br2 ( bột Fe)→ phản ứng thế vào vòng benzen vị trí o, p
X + HNO3 đặc ( xt H2SO4 đặc) → phản ứng thế vào vòng benzen vị trí o, p
Lời giải :
Gọi CTPT của X là CxHy
MX = 3,17.29 = 92
=> 12x + y = 92 (1)
Từ (1) và (2) => x = 7 và y = 8
=> CTPT của X là C7H8
X là chất lỏng, không làm mất màu dd nước brom, làm mất màu dd KMnO4 khi đun nóng => X là C6H5CH3
b)
Bài 6 trang 160 SGK Hóa học 11: Đánh dấu (+) vào ô cặp chất phản ứng với nhau theo mẫu sau:
|
|
Benzen |
Hexen |
Toluen |
Etilen |
|
H2, xúc tác Ni |
+ |
+ |
|
|
|
Br2 (dung dịch) |
|
|
|
|
|
Br2 có Fe, to |
|
|
|
|
|
Dung dịch KMnO4,to |
|
|
|
|
|
HBr |
|
|
|
|
|
H2O (xt H+) |
|
|
|
|
Lời giải :
|
|
Benzen |
Hexen |
Toluen |
Etilen |
|
H2, xúc tác Ni |
+ |
+ |
+ |
+ |
|
Br2 (dung dịch) |
|
+ |
|
+ |
|
Br2 có Fe, to |
+ |
|
+ |
|
|
Dung dịch KMnO4,to |
|
+ |
+ |
+ |
|
HBr |
|
+ |
|
+ |
|
H2O (xt H+) |
|
+ |
|
+ |
Bài 7 trang 160 SGK Hóa học 11: Cho benzen tác dụng với lượng dư HNO3 đặc có xúc tác H2SO4 đặc để điều chế nitrobenzen. Tính khối lượng nitrobenzen thu được khi dùng 1,00 tấn benzen với hiệu suất 78%.
Phương pháp giải :
Viết PTHH xảy ra, tính toán khối lượng nitrobenzen theo khối lượng phản ứng của benzen.
C6H6 + HNO3 đặc C6H5NO2 + H2O
=> mbenzen pư =?
=> mnitrobenzen =?
Lời giải :
Vì %H =78% => Khối lượng C6H6 tham gia phản ứng là:
C6H6 + HNO3 đặc C6H5NO2 + H2O
Theo PT: 78 (gam) 123 (gam)
Hay 78 (tấn ) → 123 (tấn)
Vậy theo ĐB: 0,78 (tấn) → x (tấn)
=> (tấn)
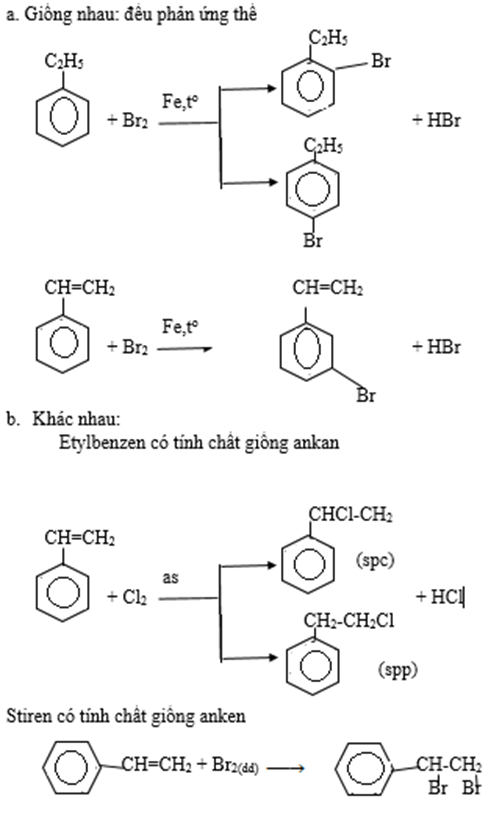
Bài 8 trang 160 SGK Hóa học 11: So sánh tính chất hóa học của etylbenzen với stiren, viết phương trình hóa học của các phản ứng để minh họa.
Lời giải :
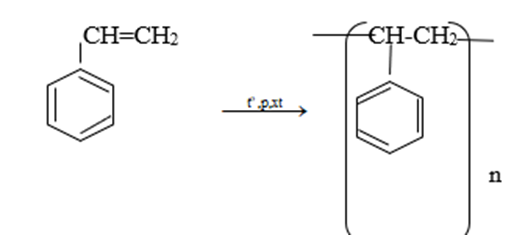
Bài 9 trang 160 SGK Hóa học 11:Dùng công thức cấu tạo viết phương trình hóa học của phản ứng giữa stiren với:
a) H2O (xúc tác H2SO4)
b) HBr
c) H2 (theo tỉ lệ số mol 1:1, xúc tác Ni)
Phương pháp giải :
Stiren có CTCT là: C6H5CH=CH2
Ghi nhớ: quy tắc cộng zaixep khi tác nhân cộng không đối xứng
a) HOH cộng vào liên kết đôi C=C với sản phẩm chính là H vào cacbon bậc thấp ( chứa nhiều H hơn) cho sản phẩm chính
b) tương tự a
c) Cộng H2 tỉ lệ 1: 1 chỉ cộng vào liên kết C=C
Lời giải :
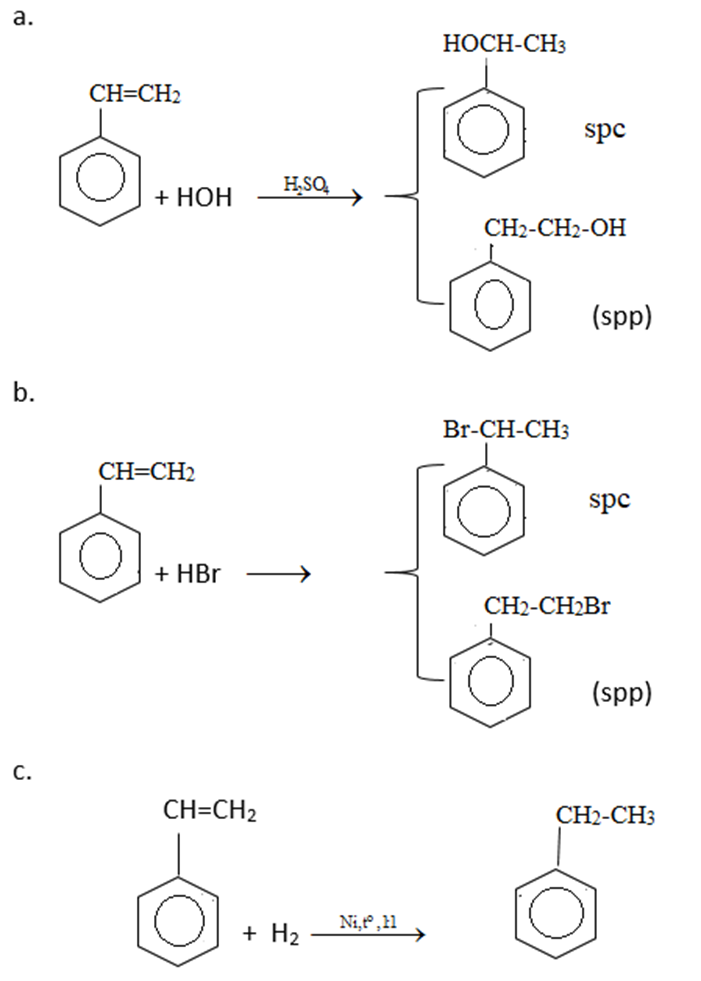
Bài 10 trang 160 SGK Hóa học 11: Trình bày phương pháp hóa học phân biệt 3 chất lỏng sau: toluen, benzen, stiren. Viết phương trình hóa học của các phản ứng đã dùng.
Phương pháp giải :
Dùng dung dịch KMnO4
ở điều kiên thường stiren làm mất màu dd thuốc tím => nhận ra được stirren
Khi đun nóng thì toluen làm mất màu dd thuốc tím => nhận ra toluen
Còn lại là benzen
Lời giải:
Cho 3 chất lỏng tác dụng với dung dịch KMnO4 ở nhiệt độ thường, chất nào làm mất màu dung dịch KMnO4 ở nhiệt độ thường là stiren.
– Với 2 hỗn hợp phản ứng còn lại ta đem đun nóng, chất nào làm mất màu dung dịch KMnO4(nóng) thì là toluen, còn lại là benzen.
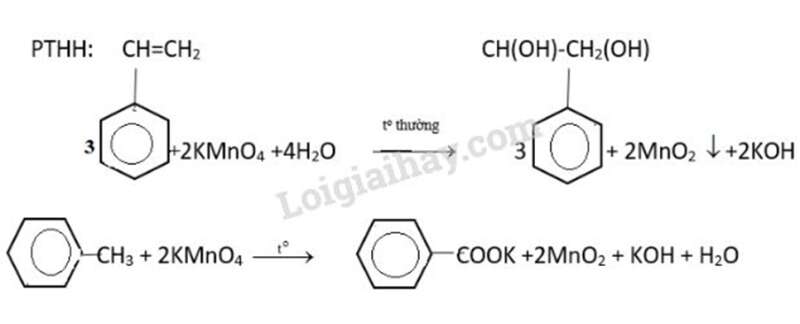
Bài 11 trang 160 SGK Hóa học 11: Khi tách hiđro của 66,25 kg etylbenzen thu được 52 kg stiren. Tiến hành phản ứng trùng hợp toàn bộ lượng stiren này thu được hỗn hợp A gồm polistiren và phần stiren chưa tham gia phản ứng. Biết 5,2 gam A vừa đủ làm mất màu của 60.00 ml dung dịch brom 0,15 M.
a)Tính hiệu suất của phản ứng tách hiđro của etylbezen.
b) Tính khối lượng stiren đã trùng hợp.
c) Polistiren có phân tử khối trung bình bằng 3,12.105. Tính hệ số trùng hợp trung bình của polime.
Phương pháp giải:
Tính sô mol của etybenzen, stiren
a) %H = (số mol stiren/ số mol etylbenzen).100%
b) Từ mol Brom => số mol của stiren dư trong 5,2 g. Từ đó suy ra được khối lượng stiren dư trong 52 kg
=> Khối lượng stiren pư = 52 – m stiren dư
c) Hệ số trùng hợp polime
Lời giải:

nStire dư = nBr2 = 0,009 (mol) => mSitren dư = 0,009.104 = 0,936 (g)
Theo định luật bảo toàn khối lượng: mtrước = msau => mA = mstiren = 52 (kg)
Cứ 5,2 gam A thì khối lượng stiren dư là 0,936 (g)
=> 52 kg A có khối lượng stiren dư là x (gam)
=>
Vậy khối lương stiren đã tham gia phản ứng là: 52 – 9,36 = 42, 64 (kg)
c) Hệ số trùng hợp là:
Bài 12 trang 160 SGK Hóa học 11: Trình bày cách đơn giản để thu được naphtalen tinh khiết từ hỗn hợp naphtalen có lẫn tạp chất không tan trong nước và không bay hơi.
Lời giải :
Úp miệng phễu có gắn giấy đục lỗ trên hỗn hợp naphtalen và tạp chất, đun nóng, naphatalen thăng hoa tạo các tinh thể hình kim bám trên mặt giấy, thu được naphtalen tinh khiết.
Bài 13 trang 161 SGK Hóa học 11: Từ etilen và benzen, tổng hợp được stiren theo sơ đồ:
C6H6 C6H5CH2CH3 C6H5CH = CH2
a) Viết các phương trình hóa học thực hiện các biến đổi trên.
b) Tính khối lượng stiren thu được từ 1,00 tấn benzen nếu hiệu suất của quá trình là 78%.
Phương pháp giải:
a)
C6H6 + C2H4 C6H5 – CH2 – CH3
C6H5CH2CH3 C6H5CH = CH2 + H2
b)
Từ PTHH: tính số mol stiren theo số mol của benzen => m stiren =?
Lời giải :
a) C6H6 + C2H4 C6H5 – CH2 – CH3
C6H5CH2CH3 C6H5CH = CH2 + H2
b) Theo sơ đồ: C6H6 → C6H5CH2CH3 → C6H5CH = CH2
nStiren = nC6H6 pư = 104 (mol)
=> mStiren = 104. 104 = 1040000 (g) = 1,04 (tấn)
Lý thuyết Benzen và đồng đẳng. Một số hiđrocacbon thơm khác
I. ĐỒNG ĐẰNG, ĐỒNG PHÂN, DANH PHÁP, CẤU TẠO
1. Đồng đằng
– Công thức chung dãy đồng đẳng của benzen: CnH2n-6 (n ≥ 6)
– Tên gọi chung là aren.
– Công thức đơn giản nhất là benzen (C6H6).
– Các ankyl benzen thương gặp là toluen C6H5CH3, xilen C6H4(CH3)2, cumen C6H5CH(CH3)2, …
2. Danh pháp
– Khi coi vòng benzen là mạch chính thì các nhóm ankyl đính với nó là mạch nhánh (còn gọi là nhóm thế).
– Tên gọi: Tên vị trí – tên nhánh + benzen
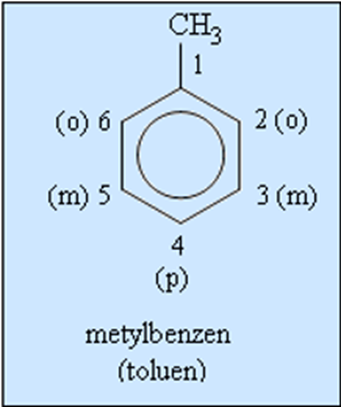
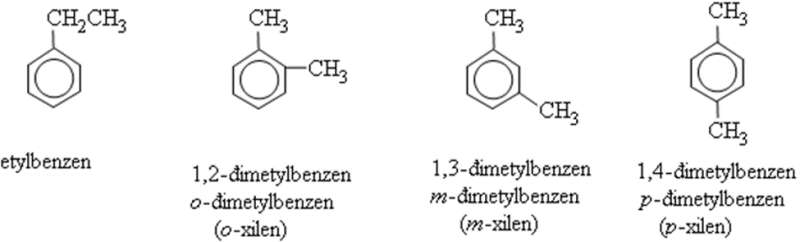
3. Đồng phân
– Đồng phân gồm: Đồng phân vị trí nhóm ankyl trong vòng benzen và đồng phân mạch cacbon của nhánh.
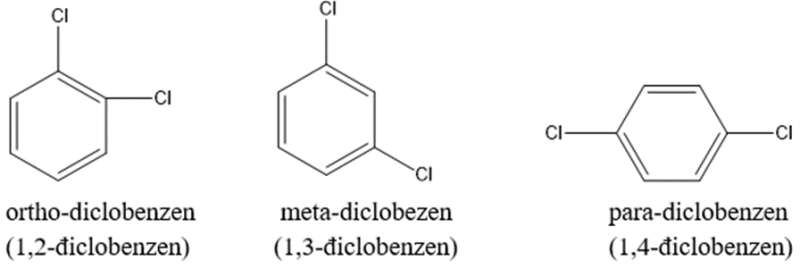
+ Nếu 2 nhóm thế ở 2 C lân cận ta có đồng phân ortho (viết tắt o-) hoặc đánh số 1,2.
+ Nếu 2 nhóm thế cách nhau 1 nguyên tử cacbon (1 đỉnh tam giác) gọi là đồng phân meta (viết tắt m-) hoặc 1,3.
+ Nếu 2 nhóm thế ở 2 nguyên tử cacbon đối đỉnh gọi là đồng phân para (viết tắt p-) hoặc 1,4.
Ví dụ: Các đồng phân của diclobenzen (C6H4Cl2).
4. Cấu tạo
– Cấu trúc phân tử benzen: Sáu nguyên tử C trong phân tử liên kết với nhau tạo vòng 6 cạnh, 3 liên kết đôi tạo hệ liên hợp chung cho cả vòng benzen. Các nguyên tử trong phân tử cùng nằm trên mặt phẳng.
– Biểu diễn cấu tạo benzen:
![]()
II. TÍNH CHẤT VẬT LÍ
Bezen là chất lỏng, không màu, có mùi thơm đặc trưng, nhẹ hơn nước và không tan trong nước nhưng tan nhiều trong dung môi hữu cơ như rượu, ete, xeton
III. TÍNH CHẤT HÓA HỌC
1. Phản ứng thế
– Phản ứng thế H ở nhân thơm bởi các tác nhân như halogen X2/Fe; HNO3/H2SO4 đặc… tuân theo quy tắc thế vào vòng benzen.
C6H6 + Br2 → C6H5Br + HBr (Fe, tº)
C6H6 + HNO3 → C6H5NO2 + H2O (H2SO4 đặc, tº)
– Quy tắc thế vào vòng benzen:
+ Nếu vòng benzen đã có sẵn nhóm thế loại I (-OH, ankyl, -NH2, …) thì phản ứng thế xảy ra dễ hơn so với benzen và ưu tiên thế vào vị trí o- và p-.
+ Nếu vòng benzen đã có sẵn nhóm thế loại II (-COOH, -CHO, -CH=CH2) thì phản ứng thế xảy ra khó hơn so với benzen và ưu tiên thế vào vị trí m-.
2. Phản ứng cộng: R
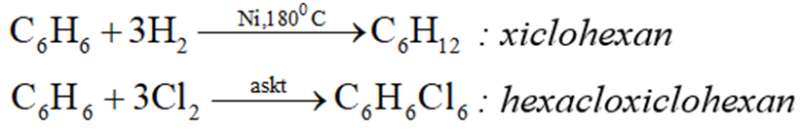
3. Phản ứng oxi hóa
– Phản ứng cháy tỏa nhiều nhiệt và cho nhiều muội than.
– Benzen không làm mất màu KMnO4
– Ankylbenzen tác dụng với dung dịch KMnO4/to (hoặc K2Cr2O7) bị oxi hóa không hoàn toàn nhóm ankyl, trong đó CH3 chuyển thành nhóm – COOH.
C6H5-CH3 + 2KMnO4 → C6H5COOK + 2MnO2 + KOH + H2O
IV. STIREN C8H8 (hay: vinybenzen, phenyletilen)
– Stiren là chất lỏng không màu, nhẹ hơn nước, không tan trong nước.
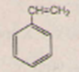
– Tính chất hóa học:
+ Tính chất thơm tương tự ankylbenzen: có phản ứng thế H ở nhân thơm, oxi hóa Cα ở nhánh.
+ Tính chất không no của nhóm vinyl tương tự anken: cộng halogen, cộng hiđro halogenua, trùng hợp, làm mất màu dung dịch KMnO4.
V. NAPHTALEN
– CTPT C10H8 và có công thức cấu tạo
![]()
– Naphtalen là chất rắn màu trắng, thăng hoa ngay ở nhiệt độ thường, có mùi đặc trưng, không tan trong nước, tan trong dung môi hữu cơ.
– Naphtalen có tính thơm tương tự benzen: Naphtalen tham gia từng phản ứng thế dễ dàng hơn benzen và thường ưu tiên thế nguyên tử H ở vị trí Cα (vị trí C số 1 của vòng), có phản ứng cộng H2/(Ni, to) tạo C10H12 (tralin) hoặc C10H18 (đecanlin).
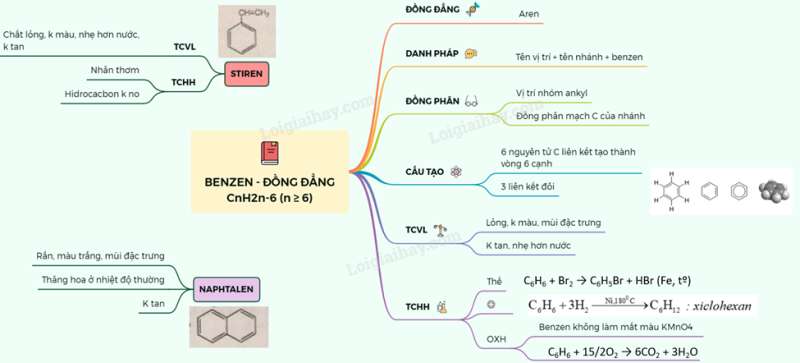
Sơ đồ tư duy: Benzen và đồng đẳng. Một số hiđrocacbon thơm khác