Giải bài tập Hóa học lớp 10 Bài 5: Lớp, phân lớp và cấu hình electron
Giải hóa học 10 trang 26 Cánh diều
Mở đầu trang 26 Hóa học 10: Cho biết sự phân bố electron theo lớp của các nguyên tử H, He, Li như sau:
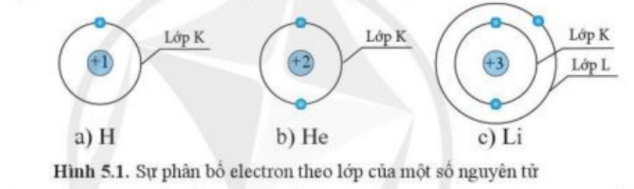
Dựa vào hình 5.1, hãy cho biết số electron tối đa ở lớp K của các nguyên tử có số hiệu nguyên tử Z 2 là bao nhiêu. Theo em, thứ tự phân bố electron vào lớp vỏ nguyên tử như thế nào?
Phương pháp giải:
Số electron tối đa trong mỗi lớp là 2n2(n là số thứ tự lớp n 4).
Lời giải:
– Số electron tối đa ở lớp K của các nguyên tử có số hiệu nguyên tử tử Z 2 là
– Thứ tự phân bố electron vào lớp vỏ nguyên tử
+ Các electron được phân bố vào lớp gần hạt nhân trước.
+ Số electron tối đa trong mỗi lớp là 2n2(n là số thứ tự lớp n 4).
I. Lớp và phân lớp electron
Câu hỏi 1 trang 26 Hóa học 10: Vì sao số AO trong một lớp luôn bằng một nửa số electron tối đa thuộc lớp đó?
Phương pháp giải:
– Lớp thứ n có n2 AO.
– Lớp thứ n có tối đa 2n2 electron.
Lời giải:
Vì lớp thứ n có n2 AO và số electron tối đa trong mỗi lớp là 2n2 nên số AO trong một lớp luôn bằng một nửa số electron tối đa thuộc lớp đó.
Giải hóa học 10 trang 27 Cánh diều
Luyện tập 1 trang 27 Hóa học 10: Lớp ngoài cùng của nitrogen (Z = 7) có bao nhiêu electron, bao nhiêu AO?
Phương pháp giải:
Lời giải:
N (Z = 7)
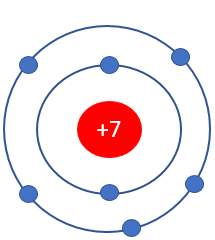
+ Lớp K có 2 electron.
+ Lớp L có 5 electron.
⇒ Lớp ngoài cùng có 5 electron và 3 AO.
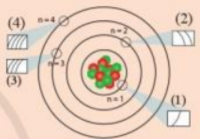
Câu hỏi 2 trang 27 Hóa học 10: Các ô (1), (2), (3), (4) trong hình dưới đây liên hệ với nội dung nào về cấu tạo lớp vỏ nguyên tử?
Phương pháp giải:
Lớp electron thứ n có n phân lớp:
+ n = 1, lớp K: có 1 phân lớp (1s).
+ n = 2, lớp L: có 2 phân lớp (2s và 2p).
+ n = 3, lớp M: có 3 phân lớp (3s, 3p và 3d).
+ n = 4, lớp N: có 4 phân lớp (4s, 4p, 4d, 4f).
Lời giải:
Ô (1): Lớp K.
Ô (2): Lớp L.
Ô (3): Lớp M.
Ô (4): Lớp N.
Câu hỏi 3 trang 27 Hóa học 10: Lớp electron thứ tư (n = 4) có bao nhiêu phân lớp và kí hiệu các phân lớp này là gì?
Phương pháp giải:
Lớp electron thứ n có n phân lớp:
+ n = 1, lớp K: có 1 phân lớp (1s).
+ n = 2, lớp L: có 2 phân lớp (2s và 2p).
+ n = 3, lớp M: có 3 phân lớp (3s, 3p và 3d).
+ n = 4, lớp N: có 4 phân lớp (4s, 4p, 4d, 4f).
Lời giải:
Lớp electron thứ tư (n = 4) có 4 phân lớp và kí hiệu là 4s, 4p, 4d, 4f.
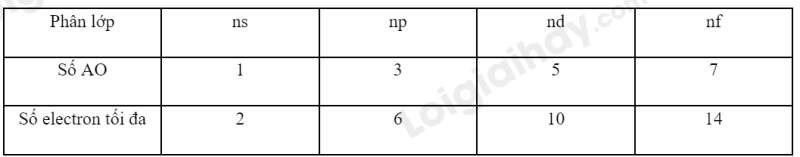
Câu hỏi 4 trang 27 Hóa học 10: Tính số electron tối đa (bão hòa) trên mỗi phân lớp ns, np, nd, nf.
Phương pháp giải:
– Số lượng AO trong mỗi phân lớp:
+ Phân lớp ns chỉ có 1 AO.
+ Phân lớp np có 3 AO.
+ Phân lớp nd có 5 AO.
+ Phân lớp nf có 7 AO.
– Số electron tối đa trong mỗi AO luôn gấp 2 lần số AO.
Lời giải:

Giải hóa học 10 trang 28 Cánh diều
II. Cấu hình electron nguyên tử
Luyện tập 2 trang 28 Hóa học 10: Viết cấu hình electron của các nguyên tố có số hiệu nguyên tử từ 1 đến 20
Phương pháp giải:
– Điền electron theo thứ tự mức năng lượng từ thấp đến cao (dãy Klechkovski):
1s, 2s, 2p, 3s, 4s, 3d, 4p, 5s, 4d, 5p, 6s, …
Điền electron bão hòa phân lớp trước rồi mới điền tiếp vào phân lớp sau.
– Đổi lại vị trí các phân lớp sao cho số thứ tự lớp (n) tăng dần từ trái qua phải
1s, 2s, 2p, 3s, 3d, 4s, 4p, 4d, …
Chú ý: Số electron tối đa của mỗi phân lớp.

Lời giải:
Z = 1: 1s1
Z = 2: 1s2
Z = 3: 1s22s1
Z = 4: 1s22s2
Z = 5: 1s22s22p1
Z = 6: 1s22s22p2
Z = 7: 1s22s22p3
Z = 8: 1s22s22p4
Z = 9: 1s22s22p5
Z = 10: 1s22s22p6
Z = 11: 1s22s22p63s1
Z = 12: 1s22s22p63s2
Z = 13: 1s22s22p63s23p1
Z = 14: 1s22s22p63s23p2
Z = 15: 1s22s22p63s23p3
Z = 16: 1s22s22p63s23p4
Z = 17: 1s22s22p63s23p5
Z = 18: 1s22s22p63s23p6
Z = 19: 1s22s22p63s23p64s1
Z = 20: 1s22s22p63s23p64s2
Giải hóa học 10 trang 29 Cánh diều
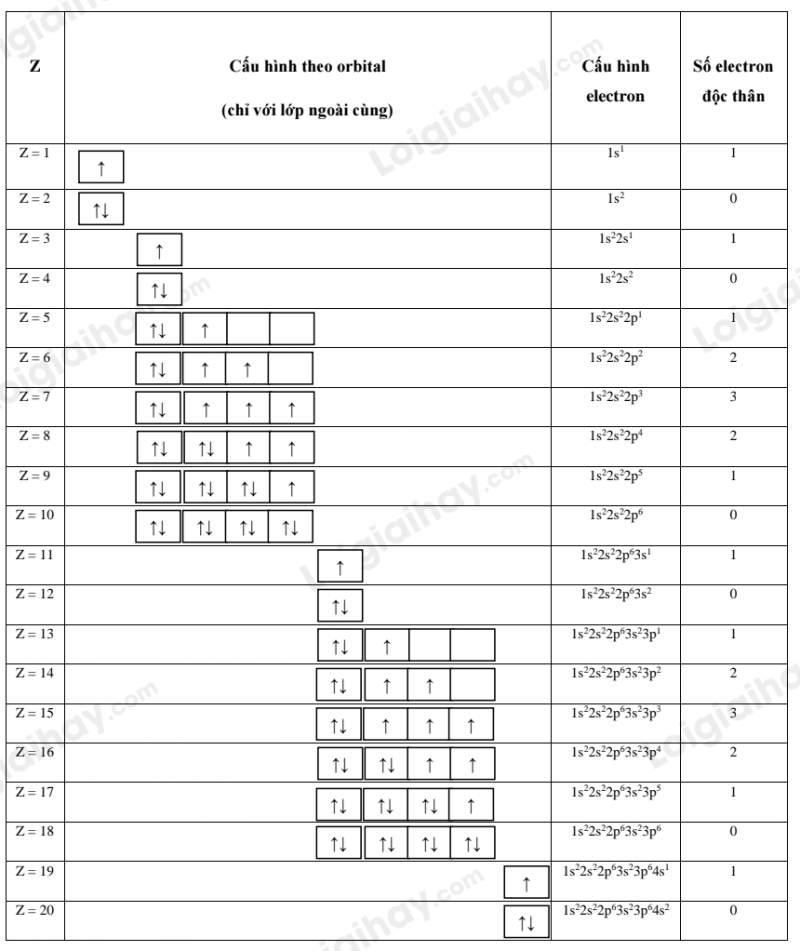
Luyện tập 3 trang 29 Hóa học 10: Biểu diễn cấu hình theo ô orbital (chỉ với lớp ngoài cùng) các nguyên tử có Z từ 1 đến 20. Xác định số electron độc thân của mỗi nguyên tử.
Phương pháp giải:
Chú ý:
+ Điền electron vào từng ô orbital theo thứ tự lớp và phân lớp.Chú ý:
+ Trong mỗi phân lớp, electron được phân bố sao cho số electron độc thân là lớn nhất.
+ Electron được điền từ trái sang phải.
+ Trong mỗi ô, electron đầu tiên được biểu diễn bằng ↑, electron thứ hai được biểu diễn bằng ↓.
Lời giải:
Giải hóa học 10 trang 30 Cánh diều
III. Dự đoán tính chất hóa học cơ bản của nguyên tố dựa theo cấu hình electron của nguyên tử
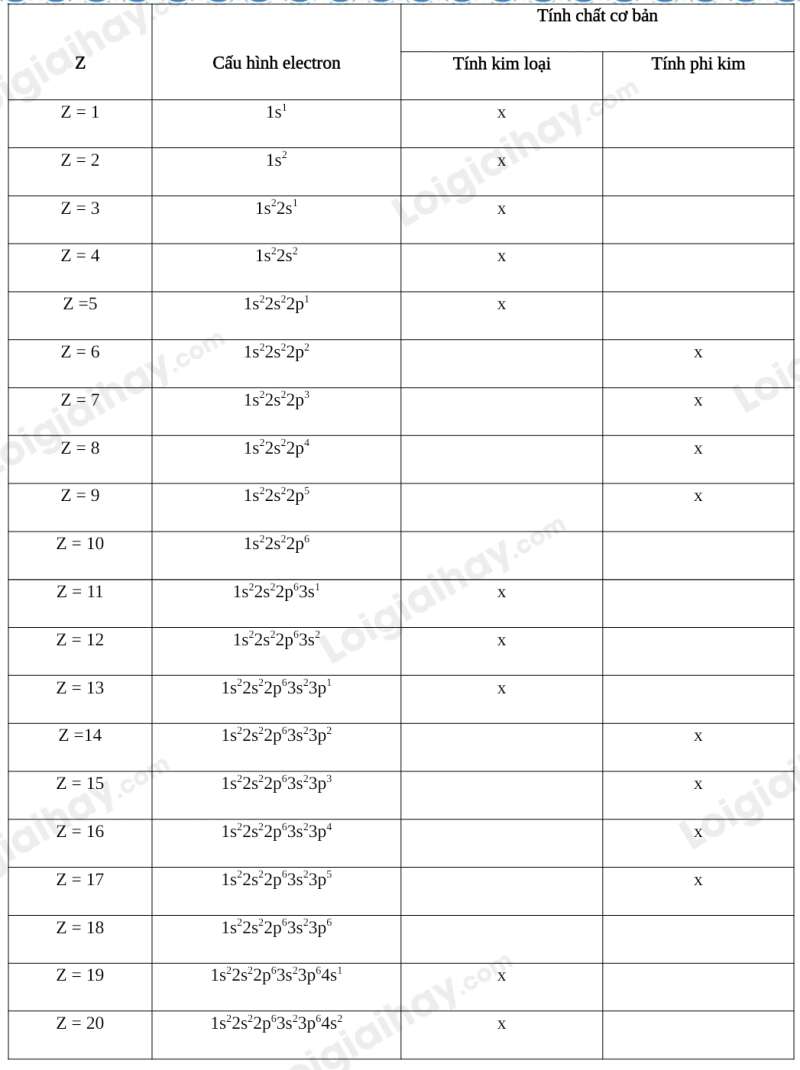
Luyện tập 4 trang 30 Hóa học 10: Dự đoán tính chất hóa học cơ bản (tính kim loại, tính phi kim) của các nguyên tố có Z từ 1 đến 20.
Phương pháp giải:
Từ cấu hình electron, có thể dự đoán các tính chất theo quy tắc sau:
Các nguyên tử có … electron ở lớp ngoài cùng
+ 1, 2, 3: nguyên tố kim loại (tính khử).
+ 5, 6, 7: nguyên tố phi kim (tính oxi hóa).
+ 8: nguyên tố khí hiếm (trừ He chỉ có 2 electron).
+ 4: nguyên tố kim loại hoặc phi kim.
Lời giải:
Bài tập (trang 30)
Bài 1 trang 30 Hóa học 10: Những phát biểu nào sau đây là đúng?
(a) Orbital 1s có dạng hình cầu, orbital 2s có dạng hình số tám nổi.
(b) Trong một nguyên tử, năng lượng của electron thuộc AO 1s thấp hơn năng lượng của electron thuộc AO 2s.
(c) Trong một nguyên tử, năng lượng của electron thuộc AO 2s thấp hơn năng lượng của electron thuộc AO 2p.
(d) Trong một nguyên tử, năng lượng của electron thuộc AO 2s gần năng lượng của electron thuộc AO 2p.
Phương pháp giải:
– AO s (AO hình cầu), AO p (AO hình số tám nổi).
– Các electron thuộc cùng một phân lớp có năng lượng bằng nhau, các electron thuộc cùng một lớp có năng lượng gần bằng nhau.
Lời giải:
(a) Sai vì AO s có dạng hình cầu.
(b) Đúng.
(c) Sai.
(d) Đúng.
Bài 2 trang 30 Hóa học 10: Nguyên tử nguyên tố X có hai lớp electron, trong đó có một electron độc thân. Vậy X có thể là những nguyên tố nào?
Lời giải:
X có hai lớp electron và có một electron độc thân
X có thể là Li (Z = 3):1s22s1 hoặc F (Z = 9): 1s22s22p5.
Bài 3 trang 30 Hóa học 10: Cấu hình electron của ion được thiết lập bằng cách thêm hoặc bớt electron, bắt đầu từ phân lớp ngoài cùng của cấu hình electron nguyên tử tương ứng.
a) Viết cấu hình electron của Na+ và Cl–.
b) Nguyên tử Cl nhận 1 electron để trở thành ion Cl–, electron này xếp vào AO thuộc phân lớp nào của Cl? AO đó là AO trống, chứa 1 hay 2 electron?
Lời giải:
a) Na (Z = 11) 1s22s22p63s1 ⇒ Na+: 1s22s22p6.
Cl (Z = 17) 1s22s22p63s23p5 ⇒ Cl–: 1s22s22p63s23p6.
b) Nguyên tử Cl nhận 1 electron để trở thành ion Cl–, electron này xếp vào AO thuộc phân lớp p của Cl. AO đó là AO chứa 1 electron.
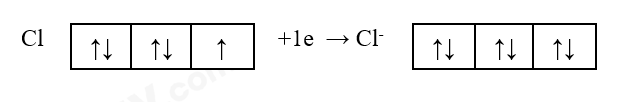
Bài giảng Hóa học 10 Bài 5: Lớp, phân lớp và cấu hình electron – Cánh diều
Xem thêm các bài giải SGK Hóa học lớp 10 Cánh diều hay, chi tiết khác:
Bài 4: Mô hình nguyên tử và orbital nguyên tử
Bài 6: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
Bài 7: Xu hướng biến đổi một số tính chất của đơn chất, biến đổi thành phần và tính chất của hợp chất trong một chu kì và trong một nhóm
Bài 8: Định luật tuần hoàn và ý nghĩa của bảng tuần hoàn các nguyên tố hóa học