Giải bài tập Hóa học lớp 10 Bài 14: Phản ứng hóa học và enthalpy
Giải hóa học 10 trang 77 Cánh diều
Mở đầu trang 77 Hóa học 10: Cho các phản ứng sau:
(1) Phản ứng nung vôi: CaCO3 → CaO + CO2
(2) Phản ứng than cháy trong không khí: C + O2 → CO2
Trong hai phản ứng trên, phản ứng nào là tỏa nhiệt, phản ứng nào là thu nhiệt?
Phương pháp giải:
Phản ứng giải phóng năng lượng dưới dạng nhiệt (phản ứng tỏa nhiệt): phản ứng đốt cháy nhiên liệu, phản ứng tạo gỉ sắt, phản ứng oxi hóa glucose trong cơ thể, …
Phản ứng hấp thụ năng lượng dưới dạng nhiệt (phản ứng thu nhiệt): phản ứng trong lò nung vôi, nung clinker xi măng, …
Lời giải:
(1) Phản ứng thu nhiệt.
(2) Phản ứng tỏa nhiệt.
Giải hóa học 10 trang 78 Cánh diều
I. Phản ứng tỏa nhiệt và phản ứng thu nhiệt
Câu hỏi 1 trang 78 Hóa học 10: Khi làm thí nghiệm, làm thế nào để biết một phản ứng là tỏa nhiệt hay thu nhiệt?
Phương pháp giải:
Phản ứng tỏa nhiệt: là phản ứng hóa học thường kèm theo sự giải phóng hoặc hấp thụ năng lượng dưới dạng nhiệt.
Phản ứng thu nhiệt: là phản ứng hóa học có sự cung cấp nhiệt cho phản ứng
Lời giải:
– Để nhận biết phản ứng tỏa nhiệt: Ta cảm nhận hoặc đo được nhiệt độ xung quanh phản ứng thí nghiệm đó tăng lên . Hoặc phản ứng không cần cung cấp nhiệt trong suốt quá trình xảy ra phản ứng
– Để nhận biết phản ứng thu nhiệt: Ta cần phải cung cấp nhiệt trong suốt quá trình xảy ra phản ứng thì phản ứng mới diễn ra
Vận dụng 1 trang 78 Hóa học 10: Dự đoán các phản ứng sau là tỏa nhiệt hay thu nhiệt?
a) Nung NH4Cl(s) tạo ra HCl(g) và NH3(g).
b) Cồn cháy trong không khí.
c) Phản ứng thủy phân collagen thành gelatin (là một loại protein dễ tiêu hóa) diễn ra khi hầm xương động vật.
Phương pháp giải:
Phản ứng giải phóng năng lượng dưới dạng nhiệt (phản ứng tỏa nhiệt): phản ứng đốt cháy nhiên liệu, phản ứng tạo gỉ sắt, phản ứng oxi hóa glucose trong cơ thể, …
Phản ứng hấp thụ năng lượng dưới dạng nhiệt (phản ứng thu nhiệt): phản ứng trong lò nung vôi, nung clinker xi măng, …
Lời giải:
a) NH4Cl(s) → HCl(g) + NH3(g)
=> Phản ứng cần cung cấp nhiệt trong suốt quá trình phản ứng => Phản ứng thu nhiệt.
b) C2H5OH + O2 → CO2 + H2O
=> Phản ứng chỉ cần cung cấp nhiệt vào thời điểm ban đầu và có tỏa nhiệt trong quá trình phản ứng => Phản ứng tỏa nhiệt.
c) Collagen → gelatin
=> Phản ứng cần cung cấp nhiệt trong suốt quá trình phản ứng (hầm) =>Phản ứng tỏa nhiệt.
Vận dụng 2 trang 78 Hóa học 10: Lấy ví dụ một số phản ứng xảy ra trong tự nhiên có kèm theo sự tỏa nhiệt hoặc thu nhiệt mà em biết.
Phương pháp giải:
– Phản ứng tỏa nhiệt: phản ứng giải phóng năng lượng dưới dạng nhiệt
– Phản ứng thu nhiệt: phản ứng hấp thụ năng lượng dưới dạng nhiệt
Lời giải:
Phản ứng tỏa nhiệt: Sulfuric acid (H2SO4) + Đường, Xăng cháy trong không khí, Củi cháy trong không khí, Phản ứng tạo gỉ sắt, Nến cháy trong không khí …
Phản ứng thu nhiệt: Băng tan, Nước lỏng bay hơi, Luộc trứng, Nấu canh, Nung gốm…
Giải hóa học 10 trang 79 Cánh diều
II. Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học
Câu hỏi 2 trang 79 Hóa học 10: Nhiệt tỏa ra khi hình thành 1 mol Na2O(s) ở điều kiện chuẩn từ phản ứng giữa Na(s) và O3(g) có được coi là nhiệt tạo thành chuẩn của Na2O(s) không? Giả sử Na tác dụng được với O3 thu được Na2O.
Phương pháp giải:
Enthalpy tạo thành chuẩn (nhiệt tạo thành chuẩn) của một chất là lượng nhiệt kèm theo của phản ứng tạo thành 1 mol chất đó từ các đơn chất ở dạngbền nhất trong điều kiện chuẩn.
Lời giải:
Nhiệt tỏa ra khi hình thành 1 mol Na2O(s) ở điều kiện chuẩn từ phản ứng giữa Na(s) và O3(g) không được coi là nhiệt tạo thành chuẩn của Na2O(s) vì oxygen dạng phân tử O3 (ozone) không là dạng bền nhất.
Câu hỏi 3 trang 79 Hóa học 10: Trong ví dụ 1, ở cùng điều kiện phản ứng, nếu chỉ thu được 0,5 mol Na2O thì lượng nhiệt tỏa ra là bao nhiêu kJ?
Phương pháp giải:
giảm khi lượng chất tạo thành giảm.
Lời giải:
2Na(s) + ½ O2(g) → Na2O(s) kJ.mol-1
Na(s) + ¼ O2(g) → ½ Na2O(s) kJ.mol-1
Câu hỏi 4 trang 79 Hóa học 10: Cho phản ứng:
N2(g) + 3H2(g) → 2NH3(g)
Ở điều kiện chuẩn, cứ 1 mol N2 phản ứng hết sẽ tỏa ra 92,22 kJ. Tính enthalpy tạo thành chuẩn của NH3.
Phương pháp giải:
Enthalpy tạo thành chuẩn (nhiệt tạo thành chuẩn) của một chất là lượng nhiệt kèm theo của phản ứng tạo thành 1 mol chất đó từ các đơn chất ở dạng bền nhất trong điều kiện chuẩn.
Lời giải:
N2(g) + 3H2(g) → 2NH3(g)
Cứ 1 mol N2 phản ứng hết tỏa ra 99,22kJ và tạo ra 2 mol NH3
=> 0,5 mol N2 phản ứng hết tỏa ra 49,61kJ và tạo ra 1 mol NH3
=> (enthalpy có giá trị âm vì đây là phản ứng tỏa nhiệt)
Câu hỏi 5 trang 79 Hóa học 10: Vì sao enthalpy tạo thành của một đơn chất bền lại bằng không?
Phương pháp giải:
Đơn chất bền: tồn tại sẵn trong điều kiện chuẩn, không cần phản ứng nào để tạo thành
Lời giải:
– Enthalpy tạo thành chuẩn của một chất là lượng nhiệt kèm theo của phản ứng tạo thành 1 mol chất đó từ các đơn chất ở dạng bền nhất trong điều kiện chuẩn
=> Đơn chất bền, không cần phản ứng nào từ đơn chất để tạo thành
=> Enthalpy tạo thành của một đơn chất bền bằng 0
Giải hóa học 10 trang 80 Cánh diều
Câu hỏi 6 trang 80 Hóa học 10: Giá trị của phản ứng sau là bao nhiêu kJ?
½ CH4(g) + O2(g) → ½ CO2(g) + H2O(l)
Phương pháp giải:
Dựa vào ví dụ (1) trang 80:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l)
tỉ lệ thuận với lượng chất tham gia và sản phẩm
Lời giải:
½ CH4(g) + O2(g) → ½ CO2(g) + H2O(l)
Luyện tập 1 trang 80 Hóa học 10: Đốt cháy hoàn toàn 1 gam C2H2(g) ở điều kiện chuẩn, thu được CO2(g) và H2O(l), giải phóng 49,98 kJ. Tính biến thiên enthalpy chuẩn của phản ứng đốt cháy 1 mol C2H2.
Phương pháp giải:
tỉ lệ thuận với lượng chất tham gia và sản phẩm
Lời giải:
nC2H2 = 1/26 (mol)
Đốt cháy 1/26 mol C2H2 tỏa ra 49,98 kJ
=> Đốt cháy 1 mol C2H2 tỏa ra x kJ
=> x = 1 x 49,98 : (1/26) = 1299,48 kJ
=> = -1299,48 kJ (vì đây là phản ứng tỏa nhiệt nên enthalpy mang giá trị âm)
Luyện tập 2 trang 80 Hóa học 10: Ở điều kiện chuẩn, cần phải đốt cháy hoàn toàn bao nhiêu gam CH4(g) để cung cấp nhiệt cho phản ứng tạo 1 mol CaO bằng cách nung CaCO3. Giả thiết hiệu suất các quá trình đều là 100%.
Phương pháp giải:
Khi đốt cháy 1 mol CH4 tỏa ra 890,36 kJ
Để tạo thành 1 mol CaO bằng cách nung CaCO3 cần 178,29kJ
Lời giải:
– Khi đốt cháy 1 mol CH4 tỏa ra 890,36 kJ
– Để tạo thành 1 mol CaO bằng cách nung CaCO3 cần 178,29kJ
=> Số mol CH4 cần dùng để đốt cháy là: 178,29 : 890,36 = 0,2 mol
=> Số gam CH4 cần dùng để đốt cháy là: 0,2 x 16 = 3,2 (gam)
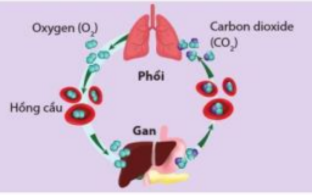
Vận dụng 3 trang 80 Hóa học 10: Sự hô hấp cung cấp oxygen cho các phản ứng oxi hóa chất béo, chất đường, tinh bột, … trong cơ thể con người. Đó là các phản ứng giải phóng hay hấp thụ năng lượng? Năng lượng kèm theo các phản ứng này dùng để làm gì?
Phương pháp giải:
Sự oxi hóa chất béo, chất đường, tinh bột…trong cơ thể con người giúp giải phóng năng lượng, cung cấp năng lượng cho các hoạt động
Lời giải:
– Sự hô hấp cung cấp oxygen cho các phản ứng oxi hóa chất béo, chất đường, tinh bột,… trong cơ thể con người đó là các phản ứng giải phóng năng lượng
– Năng lượng kèm theo các phản ứng dùng để cung cấp năng lượng cho các hoạt động
Giải hóa học 10 trang 81 Cánh diều
Bài tập (trang 81)
Bài 1 trang 81 Hóa học 10: Những loại phản ứng nào sau đây cần phải cung cấp năng lượng trong quá trình phản ứng?
(a) Phản ứng tạo gỉ kim loại
(b) Phản ứng quang hợp
(c) Phản ứng nhiệt phân
(d) Phản ứng đốt cháy
Phương pháp giải:
Phản ứng cần cung cấp năng lượng trong quá trình phản ứng là phản ứng thu nhiệt
Lời giải:
(a): Không cần cung cấp nhiệt
(b): Không cần cung cấp nhiệt
(c): Cần cung cấp nhiệt để nhiệt phân
(d): Chi cần nhiệt lúc khơi mào phản ứng
=> Phản ứng (c) là phản ứng cần cung cấp năng lượng trong quá trình phản ứng
Đáp án C
Bài 2 trang 81 Hóa học 10: Một số phản ứng khi xảy ra sẽ làm nóng môi trường xung quanh, một số khác lại làm lạnh môi trường xung quanh. Em hãy cho biết sự khác biệt cơ bản giữa hai loại phản ứng này.
Phương pháp giải:
– Phản ứng tỏa nhiệt là phản ứng giải phóng năng lượng dưới dạng nhiệt
– Phản ứng thu nhiệt là phản ứng hấp thụ năng lượng dưới dạng nhiệt
Lời giải:
– Phản ứng khi xảy ra làm nóng môi trường xung quanh => Phản ứng giải phóng năng lượng dưới dạng nhiệt => Phản ứng tỏa nhiệt
– Phản ứng khi xảy ra làm lạnh môi trường xung quanh => Phản ứng hấp thụ năng lượng dưới dạng nhiệt => Phản ứng thu nhiệt
Bài 3 trang 81 Hóa học 10: Cho biết phản ứng sau có > 0 và diễn ra ở ngay nhiệt độ phòng.
2NH4NO3(s) + Ba(OH)2.8H2O(s) → 2NH3(aq) + Ba(NO3)2(aq) + 10H2O(l)
Khi trộn đều một lượng ammonium nitrate (NH4NO3) rắn với một lượng barium hydroxide ngậm nước (Ba(OH)2.8H2O) ở nhiệt độ phòng thì nhiệt độ của hỗn hợp sẽ tăng hay giảm? Giải thích.
Phương pháp giải:
Khi phản ứng thu nhiệt thì > 0
Lời giải:
Ta có: > 0 => Đây là phản ứng thu nhiệt
=> Phản ứng sẽ hấp thụ năng lượng dưới dạng nhiệt
=> Nhiệt độ của hỗn hợp giảm
Bài 4 trang 81 Hóa học 10: Cho biết phản ứng tạo thành 2 mol HCl(g) ở điều kiện chuẩn sau đây tỏa ra 184,6 kJ:
H2(g) + Cl2(g) → 2HCl(g) (*)
Những phát biểu sau dưới đây là đúng?
A. Nhiệt tạo thành của HCl là -184,6 kJ.mol-1.
B. Biến thiên enthalpy phản ứng (*) là -184,6 kJ.
C. Nhiệt tạo thành của HCl là -92,3 kJ.mol-1.
D. Biến thiên enthalpy phản ứng (*) là -92,3 kJ.
Phương pháp giải:
– Enthalpy tạo thành chuẩn của một chất là lượng nhiệt kèm theo của phản ứng tạo thành 1 mol chất đó từ các đơn chất ở dạng bền nhất trong điều kiện chuẩn
– Phản ứng tỏa nhiệt thì enthalpy mang giá trị âm
Lời giải:
A. Sai vì đó là nhiệt tạo thành của 2 mol HCl
B. Đúng vì (*) là phản ứng tỏa nhiệt nên enthalpy mang giá trị âm
C. Đúng vì nhiệt tạo thành tỉ lệ với số mol chất tạo thành, đây là phản ứng tỏa nhiệt nên mang giá trị âm
D. Sai vì phản ứng (*) ứng với 2 mol
=> Đáp án B, C đúng
Bài giảng Hóa học 10 Bài 14: Phản ứng hóa học và enthalpy – Cánh diều
Xem thêm các bài giải SGK Hóa học lớp 10 Cánh diều hay, chi tiết khác:
Bài 13: Phản ứng oxi hóa – khử
Bài 15: Ý nghĩa và cách tính biến thiên enthalpy phản ứng hóa học
Bài 16: Tốc độ phản ứng hóa học
Bài 17: Nguyên tố và đơn chất halogen