Câu hỏi:
Tìm đa thức bậc ba f(x) = ax3 + bx2 + cx + 1 (với a ≠ 0 ) biết f(–1) = –2, f(1) = 2, f(2) = 7.
Trả lời:
f(–1) = –2 => a(–1)3 + b(–1)2 + c(–1) + 1 = –2 => –a + b – c = –3 (1)
f(1) = 2 => a . 13 + b . 12 + c . 1 + 1 = 2 => a + b + c = 1 (2)
f(2) = 7 => a . 23 + b . 22 + c . 2 + 1 = 7 => 8a + 4b + 2c = 6 => 4a + 2b + c = 3 (3)
Từ (1), (2) và (3) ta có hệ phương trình:
Giải hệ này ta được a = 1, b = –1, c = 1.
Vậy đa thức f(x) là x3 – x2 + x + 1.
====== **** mời các bạn xem câu tiếp bên dưới **** =====
- Cho mạch điện như Hình 3. Biết U = 20 V, r1 = 1 Ω, r2 = 0,5 Ω, R = 2 Ω.
Tìm cường độ dòng điện I1, I2, I trong mỗi nhánh.
Câu hỏi:
Cho mạch điện như Hình 3. Biết U = 20 V, r1 = 1 Ω, r2 = 0,5 Ω, R = 2 Ω.
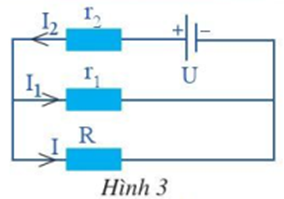
Tìm cường độ dòng điện I1, I2, I trong mỗi nhánh.
Trả lời:
Cường độ dòng điện của đoạn mạch mắc song song là: I1 + I.
Ta có: I2 = I1 + I hay I + I1 – I2 = 0 (1).
Hiệu điện thế ở đoạn mạch mắc song song là: U’ = r1 . I1 = R . I nên
1 . I1 = 2 . I hay 2I – I1 = 0 (2).
Hiệu điện thế của cả đoạn mạch là: U = U2 + U’ nên
20 = r2 . I2 + R . I hay 2I + 0,5I2 = 20 (3).
Từ (1), (2) và (3) ta có hệ phương trình:Giải hệ phương trình, ta được
====== **** mời các bạn xem câu tiếp bên dưới **** =====
- Cho mạch điện như Hình 4. Biết U = 24 V, Ð1: 12 V – 6 W, Ð2: 12 V – 12 W, R = 3 Ω.
a) Tính điện trở của mỗi bóng đèn.
b) Tính cường độ dòng điện qua các bóng đèn và qua điện trở R.
Câu hỏi:
Cho mạch điện như Hình 4. Biết U = 24 V, Ð1: 12 V – 6 W, Ð2: 12 V – 12 W, R = 3 Ω.
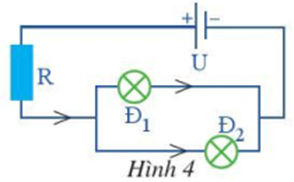
a) Tính điện trở của mỗi bóng đèn.
b) Tính cường độ dòng điện qua các bóng đèn và qua điện trở R.Trả lời:
a) Điện trở của Đ1 là: R1 =
Điện trở của Đ2 là: R2 =
b) Gọi cường độ dòng điện qua điện trở R và các bóng đèn Đ1, Đ2 lần lượt là I, I1, I2 (ampe).
Cường độ dòng điện của đoạn mạch mắc song song là: I1 + I2.
Ta có: I = I1 + I2 hay I – I1 – I2 = 0 (1).
Hiệu điện thế ở đoạn mạch mắc song song là: U’ = R1 . I1 = R2 . I2 nên
24 . I1 = 12 . I2 hay 2I1 – I2 = 0 (2).
Hiệu điện thế của đoạn mạch là: U = UR + U’ nên
24 = R . I + R1 . I1 suy ra 3I + 24I1 = 24, hay I + 8I1 = 8 (3).
Từ (1), (2) và (3) ta có hệ phương trình:
Giải hệ phương trình, ta được====== **** mời các bạn xem câu tiếp bên dưới **** =====
- Tìm các hệ số x, y, z để cân bằng mỗi phương trình sau:
a) xKClO3 →t° yKCl + zO2;
b) xFeCl2 + yCl2 →t° zFeCl3;
c) xFe + yO2 →t° zFe2O3;
d) xNa2SO3 + 2KMnO4 + yNaHSO4 →t° zNa2SO4 + 2MnSO4 + K2SO4 + 3H2O.
Câu hỏi:
Tìm các hệ số x, y, z để cân bằng mỗi phương trình sau:
a) xKClO3 yKCl + zO2;
b) xFeCl2 + yCl2 zFeCl3;
c) xFe + yO2 zFe2O3;
d) xNa2SO3 + 2KMnO4 + yNaHSO4 zNa2SO4 + 2MnSO4 + K2SO4 + 3H2O.Trả lời:
a) Theo định luật bảo toàn nguyên tố với K, Cl và O, ta có:
x = y hay x – y = 0 và 3x = 2z hay 3x – 2z = 0.
Ta có hệ phương trình:
Chọn z = 3. Khi đó hệ (1) trở thành
Vậy ta có phương trình sau cân bằng: 2KClO3 2KCl + 3O2.
a) Theo định luật bảo toàn nguyên tố với K, Cl và O, ta có:
x = y hay x – y = 0 và 3x = 2z hay 3x – 2z = 0.
Ta có hệ phương trình:
Chọn z = 3. Khi đó hệ (1) trở thành
b) Theo định luật bảo toàn nguyên tố với Fe và Cl, ta có:
x = z hay x – z = 0 và 2x + 2y = 3z hay 2x + 2y – 3z = 0.
Ta có hệ phương trình:
Chọn z = 2. Khi đó hệ (1) trở thành
Vậy ta có phương trình sau cân bằng: 2FeCl2 + Cl2 2FeCl3.
c) Theo định luật bảo toàn nguyên tố với Fe và O, ta có:
x = 2z hay x – 2z = 0 và 2y = 3z hay 2y – 3z = 0.
Ta có hệ phương trình:
Chọn z = 2. Khi đó hệ (1) trở thành
Vậy ta có phương trình sau cân bằng: 4Fe + 3O2 2Fe2O3.
c) Theo định luật bảo toàn nguyên tố với Na, H và O, ta có:
2x + y = 2z hay 2x + y – 2z = 0;
y = 6;
3x + 8 + 4y = 4z + 15 hay 3x + 4y – 4z = 7.
Ta có hệ phương trình:
Giải hệ phương trình này ta được x = 5, y = 6, z = 8.
Vậy ta có phương trình sau cân bằng:
5Na2SO3 + 2KMnO4 + 6NaHSO4 8Na2SO4 + 2MnSO4 + K2SO4 + 3H2O.====== **** mời các bạn xem câu tiếp bên dưới **** =====
- Một giáo viên dạy Hoá tạo 1000 g dung dịch HCl 25% từ ba loại dung dịch HCl có nồng độ lần lượt là 10%, 20% và 30%. Tính khối lượng dung dịch mỗi loại. Biết rằng lượng HCl có trong dung dịch 10% bằng 14 lượng HCl có trong dung dịch 20%.
Câu hỏi:
Một giáo viên dạy Hoá tạo 1000 g dung dịch HCl 25% từ ba loại dung dịch HCl có nồng độ lần lượt là 10%, 20% và 30%. Tính khối lượng dung dịch mỗi loại. Biết rằng lượng HCl có trong dung dịch 10% bằng lượng HCl có trong dung dịch 20%.
Trả lời:
Gọi khối lượng dung dịch HCl có nồng độ 10%, 20% và 30% lần lượt là x, y, z (g).
Theo đề bài ta có: x + y + z = 1000 (1).
Vì dung dịch mới có nồng độ 25% nên ta có:
Lượng HCl có trong dung dịch 10% bằng lượng HCl có trong dung dịch 20%
Từ (1), (2) và (3) ta có hệ phương trình:
Giải hệ này ta được x = 125, y = 250, z = 625.
Vậy khối lượng dung dịch HCl có nồng độ 10%, 20% và 30% lần lượt là 125 g, 250 g, 625 g.====== **** mời các bạn xem câu tiếp bên dưới **** =====
- Tổng số hạt p, n, e trong hai nguyên tử kim loại A và B là 177. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 47. Số hạt mang điện của nguyên tử B nhiều hơn của nguyên tử A là 8. Xác định số hạt proton trong một nguyên tử A.
Câu hỏi:
Tổng số hạt p, n, e trong hai nguyên tử kim loại A và B là 177. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 47. Số hạt mang điện của nguyên tử B nhiều hơn của nguyên tử A là 8. Xác định số hạt proton trong một nguyên tử A.
Trả lời:
Gọi ZA, NA lần lượt là số lượng hạt p, n của nguyên tử A.
ZB, NB lần lượt là số lượng hạt p, n của nguyên tử B.
Theo đề bài:
– Tổng số hạt p, n, e trong hai nguyên tử kim loại A và B là 177 nên ta có:
(2ZA + NA) + (2ZB + NB) = 177 (1).
– Số hạt mang điện nhiều hơn số hạt không mang điện là 47 nên ta có:
(2ZA + 2ZB) – (NA + NB) = 47 (2).
– Số hạt mang điện của nguyên tử B nhiều hơn của nguyên tử A là 8 nên ta có:
2ZB – 2ZA = 8 hay ZB – ZA = 4 (3).
Cộng theo từng vế của (1) với (2) ta được: 4ZA + 4ZB = 224 hay ZA + ZB = 56 (4).
Từ (3) và (4) ta có hệ phương trình:
Giải hệ này ta được ZA = 26, ZB = 30.
Vậy số hạt proton trong một nguyên tử A là 26.====== **** mời các bạn xem câu tiếp bên dưới **** =====